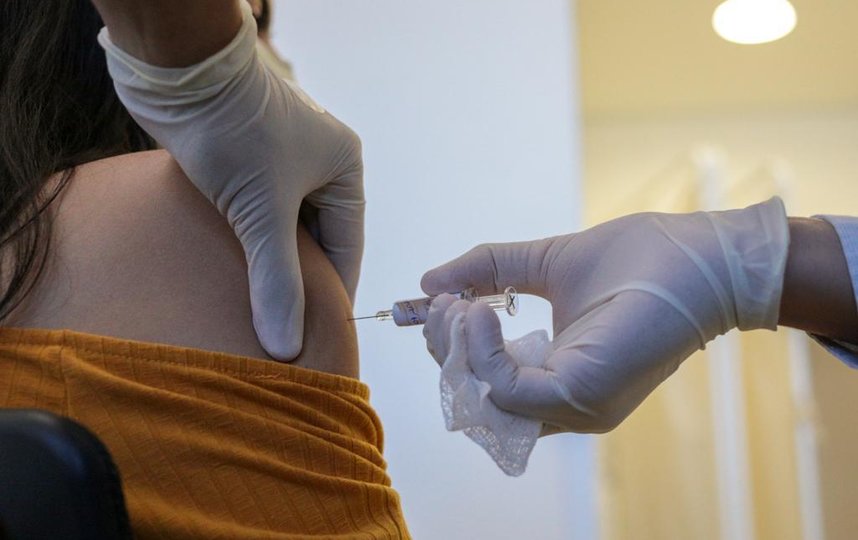
Ёксперты –осздравнадзора считают, что у фармацевтических компаний очень мало информации о российской вакцине от коронавируса.
“ак они ответили на предложение јссоциаци€ организаций по клиническим исследовани€м утверждающей, что вакцина на данном этапе небезопасна, регистрировать еЄ до успешного завершени€ третьей фазы клинических испытаний нельз€. ¬ ассоциации желание как можно быстрее свернуть разработку считают опасным пережитком.
Ќа что зам.главы –осздравнадзора ¬алентина осенко ответила, что были привиты несколько сотен добровольцев, и серьезных нежелательных реакций у них не было, передаЄт –»ј "Ќовости".
ѕо еЄ словам, в третьей фазе исследований вакцины нужно участие нескольких тыс€ч добровольцев такие обширные клинические исследовани€ в услови€х пандемии COVID-19 могут продолжатьс€ и после регистрации препарата.
“акже осенко подчеркнула, что учитыва€ богатый опыт –оссии в разработках вакцин, сомневатьс€ в качестве вакцины от коронавируса не стоит. "ќна будет соответствовать установленным требовани€м", – подчЄркивает зам.главы ведомства.
Ќапомним, над запуском производства первой в –оссии вакцины на основе аденовируса активно работают –‘ѕ» и Ќ»÷ имени √амалеи. —ейчас она проходит клинические испытани€, начатые 18 июн€, в них прин€ли участие 38 добровольцев. ¬ результате исследований удалось подтвердить безопасность вакцины, а у всех испытывающих выработалс€ иммунитет к инфекции. ѕервую группу добровольцев выписали 15 июл€, вторую – 20 июл€.
÷ентр имени √амалеи также провел испытани€ вместе с ћинобороны. ќбследование добровольцев на 42-й день после вакцинации показало, что у всех участников выработалс€ €вный иммунный ответ, никаких побочных эффектов не вы€вилось.
–оссийские власти планируют начать вакцинацию населени€ в окт€бре. ѕервыми препарат получат медики и пожилые люди.
ѕрофессор перечислил все противопоказани€ к вакцине от коронавируса